Proseguiamo il nostro excursus in merito alla patologia coronarica/ischemica; dopo aver accennato brevemente all'eziologia ed ai meccanismi fisiopatologici (Capitolo 2.6.1) ed esserci soffermati sulla angina cronica stabile (Capitolo 2.6.2), parliamo della sindrome coronarica acuta. Le sindromi ischemiche acute sono un gruppo eterogeneo di patologie, differenti sia sua base fisiopatologica che clinica, che vengono accomunate sulla base di una prognosi peggiore rispetto all’angina cronica stabile. Si usa il termine “instabilità” nel senso di “non prevedibilità”, dato che non è possibile prevedere quando si manifesteranno tali sindrome e, una volta comparse, non é possibile prevedere quale sarà la loro evoluzione.
DEFINIZIONI:
Le sindromi coronariche acute vengono definite come angor di nuova insorgenza (o come un peggioramento della sintomatologia anginosa precedente e/o come un angor che compare entro 24 ore post-infarto miocardico acuto), la cui comparsa é indipendente dall’attività fisica. Le angine instabili sono legate a meccanismi fisiopatologici differenti, ma sono accomunate da una riduzione severa del flusso coronarico, identificando quindi una popolazione a maggior rischio di infarto e di morte (che arriva fino al 10-15% ad un mese, con un rischio che ritorna nei limiti solamente a 3 mesi). Si parla di angina instabile quando si ha una delle seguenti definizioni:
- Angina a riposo: é un'angina che occorre a riposo ed in maniera prolungata, solitamente per oltre 20 minuti;
- Angina di nuova insorgenza: é una nuova angina che insorge improvvisamente, con una severità importante, pari almeno ad un grado 3 della classificazione CCS;
- Angina in crescendo: é un'angina già precedentemente diagnosticata, che diviene improvvisamente e distintamente più frequente, di maggiore durata e/o con una soglia di comparsa molto più bassa rispetto a prima.
Fatta la diagnosi di Angina Instabile, è fondamentale identificare dei sottogruppi di popolazioni che presentano un rischio di morte differente, pertanto che richiedono strategie diagnostiche e terapeutiche specifiche. Si sono pertanto identificate le popolazioni di Unstable Angina (angina instabile), danno miocardico minimo, NSTEMI e STEMI, che andremo ad analizzare prossimamente. Quando un paziente presenta le caratteristiche di instabilità anginosa, va immediatamente ricoverato c/o un reparto di cardiologia con unità coronarica ed un laboratorio di emodinamica. Sono stati proposti differenti schemi di stratificazione dell’angina instabile, solitamente il più utilizzato è quello di Braunwald che valuta il rischio a breve termine, che valuta i livelli di gravità e le circostanze cliniche donando importanti informazioni prognostiche; è fondamentale porre una corretta diagnosi differenziale fra forme primitive e secondarie (a cause extracoronariche come per anemia, ipotensione arteriosa, tachiaritmia, ecc…).
FISIOPATOLOGIA:
L’analisi degli eventi fisiopatologici permette di comprendere l’eterogeneicità della patologia, dato che - come abbiamo detto - sono differenti i meccanismi presenti in tale condizione; la presenza di taluni meccanismi (a volte combinati ad altri) permette di parlare di una condizione patologia piuttosto che un’altra.
- Occlusione meccanica: il meccanismo principale è rappresentato dalla presenza di una placca aterosclerotica che va incontro ad una progressiva, lenta e stabile evoluzione accrescitiva, con progressivo restringimento del lume vascolare e riduzione dello sforzo tollerato. Se lasciata a sé, può evolvere fino a comparire per piccoli stress (febbre, emozione, sforzo fisico lieve, ecc…) e/o a riposo.
- Occlusione dinamica: il meccanismo è rappresentato da fenomeni di vasospasmo, di entità tale da ridurre il flusso coronarico a riposo, provocando un quadro clinicamente compatibile con “angina instabile”. L’occlusione può avvenire a livello delle arterie epicardiche (sane e/o già con una placca ateromasica locale), oppure a livello delle arteriole o dei capillari (per fenomeni di vasospasmo locale); si pensa sia legato a fenomeni di ipersensibilità (congenità/acquisita) della muscolatura liscia locale e/o dei canali del calcio, con reazione abnorme a minimi stimoli vasocostrittivi. Ovviamente in caso di una placca ateromasica locale, l’entità dell’ostruzione dinamica necessaria per ridurre il flusso a tal punto da generare una sofferenza ischemica è minore rispetto all’ostruzione che è necessaria su un vaso altrimenti sano.
- Trombosi: la tendenza alla trombosi coronarica è spesso espressione di una condizione globale (diastasi trombofilica) e/o di una rottura di una placca aterosclerotica locale, con conseguente esposizione di materiale pro-trombogenico ed occlusione vascolare locale. La trombosi può andare incontro a tre destini: da un lato può esserci una fibrinolisi totale del coagulo, che compare entro i primi minuti dalla trombosi locale; può esistere anche una embolizzazione del trombo primario, con micro-occlusioni vascolari distali; può esserci una persistenza del trombo, con necrosi delle strutture vascolari localizzate a valle.
Solitamente non è uno solo dei singoli fattori a generare una sindrome coronarica acuta, ma è l’insieme di più cause (seppure con un ruolo relativo differente) a generare il danno ischemico loco-regionale. Un ruolo chiave lo gioca la placca aterosclerotica locale, per il suo rischio di divenire instabile, ma ogni singolo elemento può essere causa-conseguenza (la trombosi è causa di rottura di placca, ma può generare vasospasmo riflesso, ecc…).
DIAGNOSI:
La valutazione iniziale deve verificare se i sintomi sono provocati da ischemia miocardica e, in caso positivo, stratificare il rischio prognostico (rischio di infarto e rischio di morte), dato che tale manovra comporta una differente scelta terapeutica (si va dalla sola ASA 100 mg die PO e β-bloccanti fino al ricovero in unità coronarica).
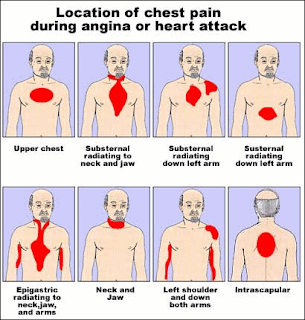
- Angor tipico: in caso di angor tipico solitamente il paziente riferisce un dolore simile ad una “oppressione” retrosternale, che può essere irradiata a livello epigastrico, alla spalla sinistra, al braccio sinistro (tipicamente sul lato ulnare), al collo ed alla mandibola. Va tenuto presente che circa un 22% dei pazienti può presentare una tipologia di dolore del tutto differente (a pugnalata, a puntura, ecc…).
- Esame obiettivo: nelle forme di angor lieve, l'esame obiettivo solitamente risulta normale in questi pazienti; si pone lo scopo di valutare se sono presenti i segni di fattori aggravanti, quali segni di scompenso cardiaco, aritmie, ecc…, oppure la presenza di fattori scatenanti come polmonite, ipertensione arteriosa non trattata, ecc… Nelle forme severe si possono manifestare segni di shock cardiocircolatorio per shock cardiogeno; in questi casi, accanto alla terapia eziologica dell'angina instabile, si deve associare la terapia di supporto per lo shock.
ELETTROCARDIOGRAMMA:
E’ un esame obbligatorio che permette di a) convalidare la diagnosi di ischemia/infarto miocardico, b) porre una corretta diagnostica differenziale fra l'angina e l'infarto miocardico e c) permette di valutare l’entità dell’ischemia. Generalmente vanno valutati i dati oggettivi di coronaropatia, quali la presenza di onde Q preesistenti, i blocchi di branca sinistra, ecc…; l’evidenza di un sovraslivellamento ST è indice di infarto transmurale, un sottoslivellamento del tratto ST di 1 mm in due derivazioni contigue è significativo se compare con il dolore, meno se persiste indipendentemente dal dolore.
Riscontrare un ECG normale rende meno probabile una diagnosi di sindrome coronarica, ma non la esclude; è fondamentale ricordarsi dei falsi negativi quando l’ischemia è troppo modesta (per dare modificazioni elettrocardiografiche), l’ischemia avviene in territori mal esplorabili (parete posteriore), l’ECG basale del paziente è alterato (e spesso non è disponibile per un confronto). La presenza di un ECG normale non esclude una coronaropatia; uno studio aveva mostrato come il 30% dei pazienti con ECG normale avesse oltre il 75% di stenosi coronarica; la derivazione D2 è generalmente la migliore per i disturbi del ritmo perché decorre parallela all'asse maggiore del cuore (quindi si hanno i segnali elettrici più ampi), mentre V5 rappresenta la derivazione più sensibile per una ischemia laterale. Un quadro comune in questi pazienti è la presenza di onde T negative che persistono nell’area interessata da ischemia; altre volte sono evidenti le onde T di Wellens, onde T negative che persistono in tutte le derivazioni precordiali (indice di una stenosi severa nell’arteria interventricolare anteriore).
Riscontrare un ECG normale rende meno probabile una diagnosi di sindrome coronarica, ma non la esclude; è fondamentale ricordarsi dei falsi negativi quando l’ischemia è troppo modesta (per dare modificazioni elettrocardiografiche), l’ischemia avviene in territori mal esplorabili (parete posteriore), l’ECG basale del paziente è alterato (e spesso non è disponibile per un confronto). La presenza di un ECG normale non esclude una coronaropatia; uno studio aveva mostrato come il 30% dei pazienti con ECG normale avesse oltre il 75% di stenosi coronarica; la derivazione D2 è generalmente la migliore per i disturbi del ritmo perché decorre parallela all'asse maggiore del cuore (quindi si hanno i segnali elettrici più ampi), mentre V5 rappresenta la derivazione più sensibile per una ischemia laterale. Un quadro comune in questi pazienti è la presenza di onde T negative che persistono nell’area interessata da ischemia; altre volte sono evidenti le onde T di Wellens, onde T negative che persistono in tutte le derivazioni precordiali (indice di una stenosi severa nell’arteria interventricolare anteriore).
Nonostante la definizione di infarto miocardico acuto / angina instabile continuino ad evolvere, la presenza dell’onda Q rimane fondamentale nel determinismo di infarti acuti/cronici, dato che permette la localizzazione dell’infarto e dell’arteria colpita, permettendo di datare l’evento. Se è vero che l'infarto miocardico acuto acuto si stratifica in STEMI/NSTEMI, è anche vero che una metodologia d’approccio moderno all’infarto miocardico acuto prevede un’ulteriore stratificazione prognostico-terapeutica in infarti Q e non-Q. Nonostante storicamente si pensasse che la presenza di onde Q fosse associata alla presenza di infarti trans murali, studi più recenti contraddicono questo, indicando che l’estensione della lesione infartuata correla con lo sviluppo di onde Q.
- Epidemiologia: lo studio è stato condotto dal 1999 al 2006 e durante questi anni si è riscontrata una progressiva riduzione delle onde Q, probabilmente per un miglioramento della velocità di accesso alle terapie riperfusorie, con riduzione della quota di infarti miocardici estesi.
- Fattori protettivi: esistono alcuni fattori che all’analisi di regressione si sono dimostrati come fattori indipendenti di protezione miocardica verso lo sviluppo di onde Q. Una pregressa coronaropatia ha un rischio relativo di 0,6 volte rispetto ai pazienti sani, probabilmente per la presenza di un pre-conditioning cronico a livello miocardico, limitando l’estensione dell’area infartuata; alcune terapie farmacologiche ad azione trombocitica o endoteliale (come l’ASA) sono in grado di ridurre l’incidenza di onde Q, e lo stesso vale per scompensi cardiaci pregressi.
- Fattori associati: esistono alcuni fattori che si sono dimostrati statisticamente più associati alla comparsa di onde Q in pazienti con sindromi coronariche acute; il diabete mellito ed il fumo sono fra i fattori più coinvolti (1,26 volte e 1,11 volte rispettivamente), probabilmente per un incremento dell’infiammazione vascolare, del rischio trombogenico e del vasospasmo associato. Anche gli interventi di PTCA e di fibrinolisi si associano alla comparsa di onde Q entro 24 ore dall’esordio (3,95 volte rispetto a popolazione di riferimento).
- Implicazioni prognostiche: i pazienti con sindromi coronariche acute e la presenza di onde Q all’ingresso in pronto soccorso generalmente presentano più facilmente quadri di scompenso cardiaco, hanno infarti di dimensioni maggiori, con picchi enzimatici maggiori, presentano arterie coronariche occluse (durante cateterizzazione) ed hanno una morbidità/mortalità intraospedaliera maggiore, quadro che si mantiene tale anche a 6 mesi. La comparsa di onde Q durante/dopo l’ospedalizzazione non sembra avere alcun impatto prognostico a 6 mesi, probabilmente perché riflette l’impatto benefico della terapia medica corrente e delle strategie riperfusorie.
ENZIMI CARDIACI:
Gli enzimi cardiaci sono enzimi contenuti all’interno della cellula miocardica, la cui rilevazione in circolo è espressione di necrosi cellulare (infarto del miocardio); gli enzimi utilizzati in tale condizione sono tre: la mioglobina, la troponina I e le CK-MB. Generalmente la clinica e l’ECG permettono di porre diagnosi immediata, ma spesso è necessario utilizzare gli enzimi per conferma e/o per diagnosi differenziale; è fondamentale conoscerne la cinetica, la sensibilità e la specificità. Il loro scopo è quello di diagnosticare l’infarto e valutarne la severità, dato che esiste una correlazione diretta fra “area sotto la curva” disegnata dagli enzimi e gravità dell’infarto. Se la clinica e l’ECG sono tipici, si inizia il trattamento SENZA attendere il risultato degli enzimi.
- Mioglobina: è l’enzima che si altera più precocemente, positiva anche dopo 1 ora, permettendo diagnosi precoci; ma non è specifico, dato che è presente anche nel muscolo scheletrico. Diviene diagnostica se associata alla clinica ed all’ECG suggestivi per infarto miocardico.
- Troponina I: è l’enzima più specifico; aumenta con maggiore latenza (circa 3 ore) e persiste per circa 1 - 2 settimane; permette di fare diagnosi certa anche dopo diversi giorni. Il suo incremento correla con la mortalità nella fase calda della malattia ed ha un valore aggiuntivo rispetto alle informazioni cliniche ed elettrocardiografiche, che correla con la precocità di elevazione del markers e con l’entità dell’elevazione.
- CK-MB: sono enzimi poco più precoci della Troponina, ma con una minore specificità rispetto alla troponina stessa; vengono anche essi utilizzati come markers prognostici in base all’area sotto la curva disegnata dal loro decorso. Data la loro precocità, un continuo incremento dei valori sierici di CK generalmente é in grado di prevedere in maniera accurata un futuro aumento dei valori di troponina.
STRATIFICAZIONE DEL RISCHIO:
I pazienti con angina instabile sospetta vanno indagati rapidamente ed in maniera efficace per determinare se il dolore toracico è dovuto ad ischemia miocardica; la diagnosi accurata e rapida permette una terapia tempestiva, dato che le possibili complicanze mortali sono soprattutto precoci. E’ fondamentale mantenere monitorati i pazienti mediante clinica/parametri emodinamici/ECG al fine di stratificare il rischio di comparsa di complicanze acute/croniche.
- Unstable Angina: è una sindrome coronarica acuta caratterizzata da alterazioni elettrocardiografiche senza positività degli enzimi cardiaci; i meccanismi fisiopatologici sono quelli delle sindromi coronariche acute.
- Danno miocardico minimo: si hanno delle alterazioni elettrocardiografiche transitorie (che scompaiono spontaneamente), seguite successivamente da un incremento della troponina I. E’ legato ad una trombosi acuta di un vaso epicardico, cui fa seguito una embolizzazione di particelle, con microinfarti distali.
- Infarto senza sovraslivellamento ST (NSTEMI): si hanno delle alterazioni elettrocardiografiche (senza sovraslivellamento del tratto ST) con alterazione degli enzimi cardiaci (sia CK-MB che Troponina I).
- Infarto con sovraslivellamento ST (STEMI): si hanno delle alterazioni elettrocardiografiche con sovraslivellamento del tratto ST, associato ad alterazione degli enzimi cardiaci.
Sulla base dell’identificazione della storia clinica (tipologia dolore, timing insorgenza ed evoluzione), dell’ECG e degli enzimi cardiaci, nel caso si sospetti una sindrome coronarica acuta, è possibile stratificare il rischio a tre livelli; permette così di decidere a) dove ricoverare il paziente (unità coronarica, terapia post-intensiva, reparto), b) la scelta del trattamento più appropriato. La valutazione del rischio va aggiornata durante il ricovero in modo tale che i pazienti ad alto rischio non vengano sottostimati e quelli a basso rischio non siano sovrastimati. I predittori più importanti sono il quadro clinico, il grado di sottoslivellamento del tratto ST durante gli attacchi, l’innalzamento della Troponina e la ricomparsa di episodi ischemici nonostante la terapia medica piena (quest’ultimo giustifica un trattamento in urgenza con coronarografia).
Si parla di rischio elevato se si ha la positività di almeno uno degli elementi contenuti nella colonna; si parla di rischio intermedio se non si ha nessun elemento a rischio elevato ma si ha almeno uno degli elementi a rischio intermedio; si parla di rischio basso se non si hanno elementi ad alto/medio rischio e si ha un elemento nella colonna a basso rischio.
- Basso rischio: sono pazienti che presentano dolori anginosi a riposo, presentano una obiettività ed un ECG normali a riposo e/o durante episodio anginoso, senza alcun movimento della Troponina.
- Medio rischio: sono pazienti anziani (over-70 anni) con anamnesi positiva per infarti e/o stroke ischemici, con dolore inferiore a 20 minuti, inversione delle onde T e minimo movimento della Troponina.
- Alto rischio: sono pazienti con episodi ripetuti di dolore nelle 48 ore precedenti, anche a riposo, della durata di oltre 20 minuti, con segni clinici di scompenso ventricolare sinistro, sottoslivellamento ST e movimento della troponina significativo.
Nonostante l’utilizzo dei migliori trattamenti attuali, esiste una quota di pazienti che nei primi mesi dopo la fase acuta di malattia va incontro a recidive di instabilità clinica, infarto e/o morte. In questi pazienti è stato dimostrato che l’infiammazione gioca un ruolo importante nella instabilizzazione della placca; in molti pazienti il processo infiammatorio si spegne dopo la fase calda di malattia, mentre in altri pazienti l’infiammazione locale persiste anche dopo la fase calda (PCR superiore a 3 mg/l) e questo permette di prevedere un incrementato rischio di recidiva e morte. I classici FANS non si sono dimostrati efficaci nel migliorare la prognosi locale, mentre le statine hanno dimostrato svolgere a dosi elevate un ruolo pleiotropo sull’infiammazione, con progressiva riduzione dei valori di PCR e di eventi avversi.
GRACE SCORE:
Il Global Registry of Acute Coronary Events (GRACE score) é basato su oltre 27.000 pazienti ed é uno score che si é dimostrato in grado di predire la mortalità ospedaliera e la mortalità alla dimissione (a 6 mesi). Come dimostrato su numerosi studi (Am J Med 2009;122(2):107) la sola Troponina non è un valore completo nella stratificazione e nel management del paziente con sindromi coronariche acute; questo per due motivi: a) la maggiore quota di pazienti con troponina positiva presenta valori che ne determinano un basso rischio globale di morte, sono pochi i pazienti con valori estremamente elevati; b) esistono pazienti con rischi elevati che possono presentare troponine negative.
Viene quindi utilizzato questo score-system che prende in considerazione l’età del paziente, la frequenza cardiaca, la Pressione Arteriosa sistolica, la creatinina, e la Kilip class, con ulteriore aggiunta di ulteriori fattori predittivi negativi (arresto cardiaco, STEMI, troponine positive). Si ottengono quindi dei punteggi che possono stratificare la mortalità ospedaliera e la mortalità a 6 mesi.
Studi recenti (JACC 2009;54:357-364) hanno dimostrato inoltre l’importanza prognostica aggiuntiva di misurazioni di altri parametri, quali possibile presenza di scompenso cardiaco (BNP), insufficienza renale (creatinina e VFG) ed infiammazione (hsCRP). Lo studio ha dimostrato che il BNP all’esordio e a 6 mesi dalla malattia è il fattore prognostico più importante nel determinismo dell’OS di questi pazienti (probabilmente perché riflette la presenza di danni miocardici di maggiori dimensioni, rimodellamenti progressivi e quindi una maggiore disfunzione ventricolare sx), mentre la hsCRP ha un ruolo prognostico solo a 6 mesi, non nella fase acuta di malattia (probabilmente perché riflette la presenza di uno stato infiammatorio a livello delle coronarie). La misurazione della VGF non si è dimostrata utile nel predirre l’outcome di questo gruppo di pazienti.
Per il NSTEMI il fattore di rischio maggiore è l'entità della elevazione della troponina; in caso di sottoslivellamento del tratto ST superiore 2 mm si ha un rischio relativo di mortalità ad 1 anno 10 volte superiore alla norma.
MANAGEMENT TERAPEUTICO:
Il paziente con unstable angina, danno miocardico minimo e/o NSTEMI viene ricoverato in unità coronarica, monitorizzato (per il rischio di alterazioni silenti del tratto ST ed aritmie cardiache), allettato a riposo e trattato mediante farmaci. I goals terapeutici sono quelli di una terapia d’attacco, spegnendo la fase di instabilità della placca (si parla di passivizzazione della placca) ed una terapia definitiva, volta a trattare definitivamente la stenosi coronarica.
TERAPIA D'ATTACCO:
Il razionale è quello di agire su tutte le componenti responsabili dell’instabilità, dall’attivazione piastrinica (farmaci anti-trombotici), alla composizione della placca aterosclerotica (statine, ASA), all’ischemia (farmaci anti-ischemici).
- Farmaci antitrombotici: sono dei farmaci che agiscono modulando il fenomeno della trombosi, fra cui ASA, Ticlopidina/Clopidogrel, gli inibitori delle glicoproteine GpIIb/IIIa e l'eparina. Nei pazienti a basso rischio è sufficiente una terapia con ASA e Clopidogrel, mentre nei pazienti ad alto rischio si devono combinare con tutti gli antitrombotici e gli anticoagulanti (Enoxaparina 1 mg/Kg bid SC), sia per l’effetto sinergico sull’attività piastrinica, che per l’effetto additivo sulla comparsa di eventi avversi (50% per infarto, chirurgia e/o morte), permettendo di eseguire PTCA durante la fase acuta. Gli effetti collaterali sono legati al rischio di sanguinamento (motivo per cui si associa una terapia preventiva con PPI). Nella fase acuta non si sono mai dimostrati rischi emorragici maggiori, mentre qualche episodio di sanguinamento minori é stato riscontrato. Periodicamente sono da controllare i trombociti per il rischio di trombocitopenia.
- Farmaci passivizzanti: la logica nell’impiego delle statine è quello di passivizzare la placca tramite la riduzione della componente lipidica e le azioni pleomorfe di tipo anti-infiammatorio; sono comunque azioni che richiedono tempo e si dimostrano utili nell'ambito della prevenzione secondaria. L’uso di alte dosi di farmaco si è dimostrato più efficace rispetto alle dosi standard, senza effetti collaterali significativi maggiori rispetto all'uso di dosi moderate. L’ASA ha lo scopo di inibire l’aggregazione piastrinica che, nel caso di angina instabile, gioca un ruolo fondamentale nel determinismo prognostico negativo del paziente; il suo utilizzo mostra effetti benefici che persistono per oltre 1 anno.
- Farmaci anti-ischemici: sono farmaci che hanno lo scopo di ridurre e prevenire l’ischemia miocardica; i nitrati sono farmaci di prima scelta per la loro maneggevolezza e l’elevata efficacia sui sintomi, anche se il tasso di responders è minore rispetto ai pazienti con angina cronica stabile; l’uso di β-bloccanti permette di ridurre il consumo di ossigeno (utile in tutti i pazienti, salvo controindicazioni); solitamente si utilizza metopropolo 5 mg/5 min IV in bolo (max 3 volte) per poi passare a 25 mg bid PO con incrementi successivi; se il paziente è a basso rischio si può iniziare già con una con terapia PO. I calcio-antagonisti centrali sono da utilizzare solamente se sono presenti controindicazioni ai β-bloccanti e/o in caso di vasospasmo come meccanismo dell’angina instabile.
TERAPIA OSPEDALIERA:
Dopo aver ottenuto la stabilizzazione clinica, con un raffreddamento della placca, sono possibili due strategie, che si sono dimostrate vantaggiose in termini di riduzione di eventi cardiovascolari maggiori. L'approccio conservativo è un approccio che non prevede l’esecuzione immediata della coronarografia, ed é un approccio che si esegue nei pazienti a basso rischio e/o a rischio intermedio che si stabilizzano con la terapia medica; si riserva la coronarografia a pazienti in cui persiste la sintomatologia nonostante la terapia medica a dose piena, oppure a pazienti con test provocativo d’ischemia positivo nonostante la terapia medica ottimale. Sono pazienti che, se non possono in alcun modo beneficiare di un trattamento invasivo, hanno una prognosi a 5 anni peggiore. Uno studio multicentrico randomizzato ha dimostrato che la terapia di rivascolarizzazione precoce in questa popolazione non porta alcun beneficio rispetto alla popolazione trattata con rivascolarizzazione tardiva.
Un approccio interventistico precoce prevede l’esecuzione di una coronarografia entro 48 ore dal ricovero, con successiva rivascolarizzazione mediante angioplastica o by-pass aorto-coronarico; attualmente, dato il miglioramento della tecnologia e la riduzione delle complicanze procedurali, si opta tendenzialmente per approcci interventistici precoci. Sempre lo studio citato prima, prevede che nella popolazione ad alto rischio (secondo GRACE-score) l'approccio interventistico precoce porti ad una riduzione della mortalità rispetto ad un approccio più tardivo.
TERAPIA DOMICILIARE:
Una volta dimesso dall’ospedale, dopo la scelta dell’approccio terapeutico più adeguato, il paziente deve proseguire la doppia antiaggregazione (ASA e Clopidogrel) per un determinato periodo di tempo (1 anno per gli stent ricoperti, 4 settimane per gli stent metallici), al fine di evitare la trombosi degli stents. Il proseguimento della terapia anti-anginosa è riservato ai pazienti che non sono stati studiati con coronarografia in fase acuta e/o in caso di rivascolarizzazione parziale. Questo ambito - altamente specialistico della Medicina Interna e della Medicina Riabilitativa rappresenta una sezione ultra-specialistica per cui si rimanda agli appositi testi che non sono parte integrante della Medicina Intensiva.
Dopo aver ottenuto la stabilizzazione clinica, con un raffreddamento della placca, sono possibili due strategie, che si sono dimostrate vantaggiose in termini di riduzione di eventi cardiovascolari maggiori. L'approccio conservativo è un approccio che non prevede l’esecuzione immediata della coronarografia, ed é un approccio che si esegue nei pazienti a basso rischio e/o a rischio intermedio che si stabilizzano con la terapia medica; si riserva la coronarografia a pazienti in cui persiste la sintomatologia nonostante la terapia medica a dose piena, oppure a pazienti con test provocativo d’ischemia positivo nonostante la terapia medica ottimale. Sono pazienti che, se non possono in alcun modo beneficiare di un trattamento invasivo, hanno una prognosi a 5 anni peggiore. Uno studio multicentrico randomizzato ha dimostrato che la terapia di rivascolarizzazione precoce in questa popolazione non porta alcun beneficio rispetto alla popolazione trattata con rivascolarizzazione tardiva.
TERAPIA DOMICILIARE:
Una volta dimesso dall’ospedale, dopo la scelta dell’approccio terapeutico più adeguato, il paziente deve proseguire la doppia antiaggregazione (ASA e Clopidogrel) per un determinato periodo di tempo (1 anno per gli stent ricoperti, 4 settimane per gli stent metallici), al fine di evitare la trombosi degli stents. Il proseguimento della terapia anti-anginosa è riservato ai pazienti che non sono stati studiati con coronarografia in fase acuta e/o in caso di rivascolarizzazione parziale. Questo ambito - altamente specialistico della Medicina Interna e della Medicina Riabilitativa rappresenta una sezione ultra-specialistica per cui si rimanda agli appositi testi che non sono parte integrante della Medicina Intensiva.
(continua...)
REFERENCES:
1. Keeley EC, Boura JA, Grines CL. Primary angioplasty versus intravenous thrombolytic therapy for acute myocardial infarction: a quantitative review of 23 randomised trials. Lancet 2003;361:13-20.
2. Mehta SR, Cannon CP, Fox KA, et al. Routine vs selective invasive strategies in patients with acute coronary syndromes: a collaborative meta-analysis of randomized trials. JAMA 2005;293:2908-17.
3. Bavry AA, Kumbhani DJ, Rassi AN, Bhatt DL, Askari AT. Benefit of early invasive therapy in acute coronary syndromes: a meta-analysis of contemporary randomized clinical trials. J Am Coll Cardiol 2006;48:1319-25.
4. Cannon CP, Gibson CM, Lambrew CT, et al. Relationship of symptom-onset-to-balloon time and door-to-balloon time with mortality in patients undergoing angioplasty for acute myocardial infarction.JAMA 2000;283:2941-7.
5. Antman EM, Hand M, Armstrong PW, et al. 2007 Focused Update of the ACC/ AHA 2004 Guidelines for the Management of Patients With ST-Elevation Myocardial Infarction: a report of the American College of Cardiology/American Heart Association Task Force on Practice Guidelines. Circulation 2008;117:296-329.
6. Fuster V, Badimon L, Badimon JJ, Chesebro JH. The pathogenesis of coronary artery disease and the acute coronary syndromes. N Engl J Med 1992;326:310-8.
7. Cannon CP, Weintraub WS, Demopoulos LA, et al. Comparison of early invasive and conservative strategies in patients with unstable coronary syndromes treated with the glycoprotein IIb/IIIa inhibitor tirofiban. N Engl J Med 2001;344: 1879-87.
8. Invasive compared with non-invasive treatment in unstable coronary-artery disease: FRISC II prospective randomised multicentre study. Lancet 1999;354:708- 15.
9. Fox KA, Poole-Wilson P, Clayton TC, et al. 5-Year outcome of an interventional strategy in non-ST-elevation acute coronary syndrome: the British Heart Foundation RITA 3 randomised trial. Lancet 2005; 366:914-20.
10. Spacek R, Widimsky P, Straka Z, et al. Value of first day angiography/angioplasty in evolving non-ST segment elevation myocardial infarction: an open multicenter randomized trial. Eur Heart J 2002;23: 230-8.
11. Neumann FJ, Kastrati A, Pogatsa-Murray G, et al. Evaluation of prolonged antithrombotic pretreatment (“cooling-off” strategy) before intervention in patients with unstable coronary syndromes: a randomized controlled trial. JAMA 2003; 290:1593-9.
12. de Winter RJ, Windhausen F, Cornel JH, et al. Early invasive versus selectively invasive management for acute coronary syndromes. N Engl J Med 2005;353:1095- 104.
13. Anderson JL, Adams CD, Antman EM, et al. ACC/AHA 2007 guidelines for the management of patients with unstable angina/non-ST-elevation myocardial infarction: a report of the American College of Cardiology/American Heart Association Task Force on Practice Guidelines (Writing Committee to Revise the 2002 Guidelines for the Management of Patients With Unstable Angina/Non-ST-Elevation Myocardial Infarction). J Am Coll Cardiol 2007;50:e1–157.
14. Bassand JP, Hamm CW, Ardissino D, et al. Guidelines for the diagnosis and treatment of non-ST-segment elevation acute coronary syndromes. Eur Heart J 2007;28:1598–660.
15. Yan AT, Yan RT, Huynh T, et al. Understanding physicians’ risk stratification of acute coronary syndromes: insights from the Canadian ACS 2 Registry. Arch Intern Med 2009;169:372–8.
16. Yan AT, Yan RT, Tan M, et al. Risk scores for risk stratification in acute coronary syndromes: useful but simpler is not necessarily better.Eur Heart J 2007;28:1072–8.
17. Lee CH, Tan M, Yan AT, et al. Use of cardiac catheterization for non-ST-segment elevation acute coronary syndromes according to initial risk: reasons why physicians choose not to refer their patients.Arch Intern Med 2008;168:291–6.
18. Owens C, McClelland A, Walsh S, Smith B, Adgey J. Comparison of value of leads from body surface maps to 12-lead electrocardiogram for diagnosis of acute myocardial infarction. Am J Cardiol 2008;102: 257– 65.
19. Savonitto S, Ardissino D, Granger CB, et al. Prognostic value of the admission electrocardiogram in acute coronary syndromes. JAMA 1999;281:707–13.
20. Welch RD, Zalenski RJ, Frederick PD, et al. Prognostic value of a normal or nonspecific initial electrocardiogram in acute myocardial infarction. JAMA 2001;286:1977– 84.
21. Cannon CP, McCabe CH, Stone PH, et al. The electrocardiogram predicts one-year outcome of patients with unstable angina and non-Q wave myocardial infarction: results of the TIMI III Registry ECG Ancillary Study. Thrombolysis in Myocardial Ischemia. J Am Coll Cardiol 1997;30:133–40.
22. Westerhout CM, Fu Y, Lauer MS, et al. Short-and long-term risk stratification in acute coronary syndromes: the added value of quantitative ST-segment depression and multiple biomarkers. J Am Coll Cardiol 2006;48:939–47.
23. Scirica BM, Morrow DA, Budaj A, et al. Ischemia detected on continuous electrocardiography after acute coronary syndrome: observations from the MERLIN-TIMI 36 (Metabolic Efficiency With Ranolazine for Less Ischemia in Non-ST-Elevation Acute Coronary Syndrome-Thrombolysis In Myocardial Infarction 36) Trial. J Am Coll Cardiol 2009;53:1411–21.
24. de Lemos JA, Antman EM, Giugliano RP, et al. Comparison of a 60-versus 90-minute determination of ST-segment resolution after thrombolytic therapy for acute myocardial infarction. In TIME-II Investigators. Intravenous nPA for Treatment of Infarcting Myocardium Early-II. Am J Cardiol 2000;86:1235–7.
25. Schröder K, Wegscheider K, Zeymer U, Tebbe U, Schröder R. Extent of ST-segment deviation in a single electrocardiogram lead 90 min after thrombolysis as a predictor of medium-term mortality in acute myocardial infarction. Lancet 2001;358:1479–86.
26. Schröder R. Prognostic impact of early ST-segment resolution in acute ST-elevation myocardial infarction. Circulation 2004;110: e506 –10.
27. La Rovere MT, Bigger JT, Jr, Marcus FI, Mortara A, Schwartz PJ. Baroreflex sensitivity and heart-rate variability in prediction of total cardiac mortality after myocardial infarction. ATRAMI (Autonomic Tone and Reflexes After Myocardial Infarction) Investigators. Lancet 1998;351:478 – 84.
28. Bauer A, Kantelhardt JW, Barthel P, et al. Deceleration capacity of heart rate as a predictor of mortality after myocardial infarction: cohort study. Lancet 2006;367:1674–81.
29. Bauer A, Malik M, Schmidt G, et al. Heart rate turbulence: standards of measurement, physiological interpretation, and clinical use: International Society for Holter and Noninvasive Electrophysiology Consensus. J Am Coll Cardiol 2008;52:1353–65.
30. Huikuri HV, Raatikainen MJ, Moerch-Joergensen R, et al. Prediction of fatal or near-fatal cardiac arrhythmia events in patients with depressed left ventricular function after an acute myocardial infarction. Eur Heart J 2009;30:689 –98.
REFERENCES:
1. Keeley EC, Boura JA, Grines CL. Primary angioplasty versus intravenous thrombolytic therapy for acute myocardial infarction: a quantitative review of 23 randomised trials. Lancet 2003;361:13-20.
2. Mehta SR, Cannon CP, Fox KA, et al. Routine vs selective invasive strategies in patients with acute coronary syndromes: a collaborative meta-analysis of randomized trials. JAMA 2005;293:2908-17.
3. Bavry AA, Kumbhani DJ, Rassi AN, Bhatt DL, Askari AT. Benefit of early invasive therapy in acute coronary syndromes: a meta-analysis of contemporary randomized clinical trials. J Am Coll Cardiol 2006;48:1319-25.
4. Cannon CP, Gibson CM, Lambrew CT, et al. Relationship of symptom-onset-to-balloon time and door-to-balloon time with mortality in patients undergoing angioplasty for acute myocardial infarction.JAMA 2000;283:2941-7.
5. Antman EM, Hand M, Armstrong PW, et al. 2007 Focused Update of the ACC/ AHA 2004 Guidelines for the Management of Patients With ST-Elevation Myocardial Infarction: a report of the American College of Cardiology/American Heart Association Task Force on Practice Guidelines. Circulation 2008;117:296-329.
6. Fuster V, Badimon L, Badimon JJ, Chesebro JH. The pathogenesis of coronary artery disease and the acute coronary syndromes. N Engl J Med 1992;326:310-8.
7. Cannon CP, Weintraub WS, Demopoulos LA, et al. Comparison of early invasive and conservative strategies in patients with unstable coronary syndromes treated with the glycoprotein IIb/IIIa inhibitor tirofiban. N Engl J Med 2001;344: 1879-87.
8. Invasive compared with non-invasive treatment in unstable coronary-artery disease: FRISC II prospective randomised multicentre study. Lancet 1999;354:708- 15.
9. Fox KA, Poole-Wilson P, Clayton TC, et al. 5-Year outcome of an interventional strategy in non-ST-elevation acute coronary syndrome: the British Heart Foundation RITA 3 randomised trial. Lancet 2005; 366:914-20.
10. Spacek R, Widimsky P, Straka Z, et al. Value of first day angiography/angioplasty in evolving non-ST segment elevation myocardial infarction: an open multicenter randomized trial. Eur Heart J 2002;23: 230-8.
11. Neumann FJ, Kastrati A, Pogatsa-Murray G, et al. Evaluation of prolonged antithrombotic pretreatment (“cooling-off” strategy) before intervention in patients with unstable coronary syndromes: a randomized controlled trial. JAMA 2003; 290:1593-9.
12. de Winter RJ, Windhausen F, Cornel JH, et al. Early invasive versus selectively invasive management for acute coronary syndromes. N Engl J Med 2005;353:1095- 104.
13. Anderson JL, Adams CD, Antman EM, et al. ACC/AHA 2007 guidelines for the management of patients with unstable angina/non-ST-elevation myocardial infarction: a report of the American College of Cardiology/American Heart Association Task Force on Practice Guidelines (Writing Committee to Revise the 2002 Guidelines for the Management of Patients With Unstable Angina/Non-ST-Elevation Myocardial Infarction). J Am Coll Cardiol 2007;50:e1–157.
14. Bassand JP, Hamm CW, Ardissino D, et al. Guidelines for the diagnosis and treatment of non-ST-segment elevation acute coronary syndromes. Eur Heart J 2007;28:1598–660.
15. Yan AT, Yan RT, Huynh T, et al. Understanding physicians’ risk stratification of acute coronary syndromes: insights from the Canadian ACS 2 Registry. Arch Intern Med 2009;169:372–8.
16. Yan AT, Yan RT, Tan M, et al. Risk scores for risk stratification in acute coronary syndromes: useful but simpler is not necessarily better.Eur Heart J 2007;28:1072–8.
17. Lee CH, Tan M, Yan AT, et al. Use of cardiac catheterization for non-ST-segment elevation acute coronary syndromes according to initial risk: reasons why physicians choose not to refer their patients.Arch Intern Med 2008;168:291–6.
18. Owens C, McClelland A, Walsh S, Smith B, Adgey J. Comparison of value of leads from body surface maps to 12-lead electrocardiogram for diagnosis of acute myocardial infarction. Am J Cardiol 2008;102: 257– 65.
19. Savonitto S, Ardissino D, Granger CB, et al. Prognostic value of the admission electrocardiogram in acute coronary syndromes. JAMA 1999;281:707–13.
20. Welch RD, Zalenski RJ, Frederick PD, et al. Prognostic value of a normal or nonspecific initial electrocardiogram in acute myocardial infarction. JAMA 2001;286:1977– 84.
21. Cannon CP, McCabe CH, Stone PH, et al. The electrocardiogram predicts one-year outcome of patients with unstable angina and non-Q wave myocardial infarction: results of the TIMI III Registry ECG Ancillary Study. Thrombolysis in Myocardial Ischemia. J Am Coll Cardiol 1997;30:133–40.
22. Westerhout CM, Fu Y, Lauer MS, et al. Short-and long-term risk stratification in acute coronary syndromes: the added value of quantitative ST-segment depression and multiple biomarkers. J Am Coll Cardiol 2006;48:939–47.
23. Scirica BM, Morrow DA, Budaj A, et al. Ischemia detected on continuous electrocardiography after acute coronary syndrome: observations from the MERLIN-TIMI 36 (Metabolic Efficiency With Ranolazine for Less Ischemia in Non-ST-Elevation Acute Coronary Syndrome-Thrombolysis In Myocardial Infarction 36) Trial. J Am Coll Cardiol 2009;53:1411–21.
24. de Lemos JA, Antman EM, Giugliano RP, et al. Comparison of a 60-versus 90-minute determination of ST-segment resolution after thrombolytic therapy for acute myocardial infarction. In TIME-II Investigators. Intravenous nPA for Treatment of Infarcting Myocardium Early-II. Am J Cardiol 2000;86:1235–7.
25. Schröder K, Wegscheider K, Zeymer U, Tebbe U, Schröder R. Extent of ST-segment deviation in a single electrocardiogram lead 90 min after thrombolysis as a predictor of medium-term mortality in acute myocardial infarction. Lancet 2001;358:1479–86.
26. Schröder R. Prognostic impact of early ST-segment resolution in acute ST-elevation myocardial infarction. Circulation 2004;110: e506 –10.
27. La Rovere MT, Bigger JT, Jr, Marcus FI, Mortara A, Schwartz PJ. Baroreflex sensitivity and heart-rate variability in prediction of total cardiac mortality after myocardial infarction. ATRAMI (Autonomic Tone and Reflexes After Myocardial Infarction) Investigators. Lancet 1998;351:478 – 84.
28. Bauer A, Kantelhardt JW, Barthel P, et al. Deceleration capacity of heart rate as a predictor of mortality after myocardial infarction: cohort study. Lancet 2006;367:1674–81.
29. Bauer A, Malik M, Schmidt G, et al. Heart rate turbulence: standards of measurement, physiological interpretation, and clinical use: International Society for Holter and Noninvasive Electrophysiology Consensus. J Am Coll Cardiol 2008;52:1353–65.
30. Huikuri HV, Raatikainen MJ, Moerch-Joergensen R, et al. Prediction of fatal or near-fatal cardiac arrhythmia events in patients with depressed left ventricular function after an acute myocardial infarction. Eur Heart J 2009;30:689 –98.












0 Response to "Sindrome coronarica acuta - Angina Instabile (Capitolo 2.6.3)"
Posting Komentar